ارتباط میکروبیوم روده و اوتیسم؛ پارادایم جدید در درمانهای ۲۰۲۵ و ۲۰۲۶
پژوهشهای اخیر بر نقش میکروبیوم روده و تأثیر آن بر سلامت مغز، بهویژه در زمینه اختلال طیف اوتیسم (ASD)، تمرکز کردهاند. مطالعات نشان میدهند که تغییرات در ترکیب میکروبیوم روده ممکن است با علائم رفتاری، شناختی و گوارشی اوتیسم مرتبط باشد.
مقدمه: چرا روده را «مغز دوم» کودکان اوتیستیک مینامیم؟
در دهههای گذشته، اختلال طیف اوتیسم (ASD) صرفاً یک چالش مغزی و سیستم عصبی پنداشته میشد. اما با ورود به سالهای ۲۰۲۵ و ۲۰۲۶، علم پزشکی با یک چرخش قهرمانانه به سمت دستگاه گوارش متمایل شده است. امروزه میدانیم که روده تنها وظیفه هضم غذا را بر عهده ندارد؛ بلکه یک اکوسیستم پیچیده بیولوژیکی شامل تریلیونها میکروارگانیسم است که مستقیماً فرماندهیِ بخشی از رفتارهای اجتماعی، سطح اضطراب و تواناییهای یادگیری را در دست دارد.
در این مقاله جامع به بررسی عمیق ارتباط میکروبیوم روده و اوتیسم میپردازیم و جدیدترین پروتکلهای درمانی جهان را که بر پایه محور روده-مغز بنا شدهاند، تحلیل میکنیم.
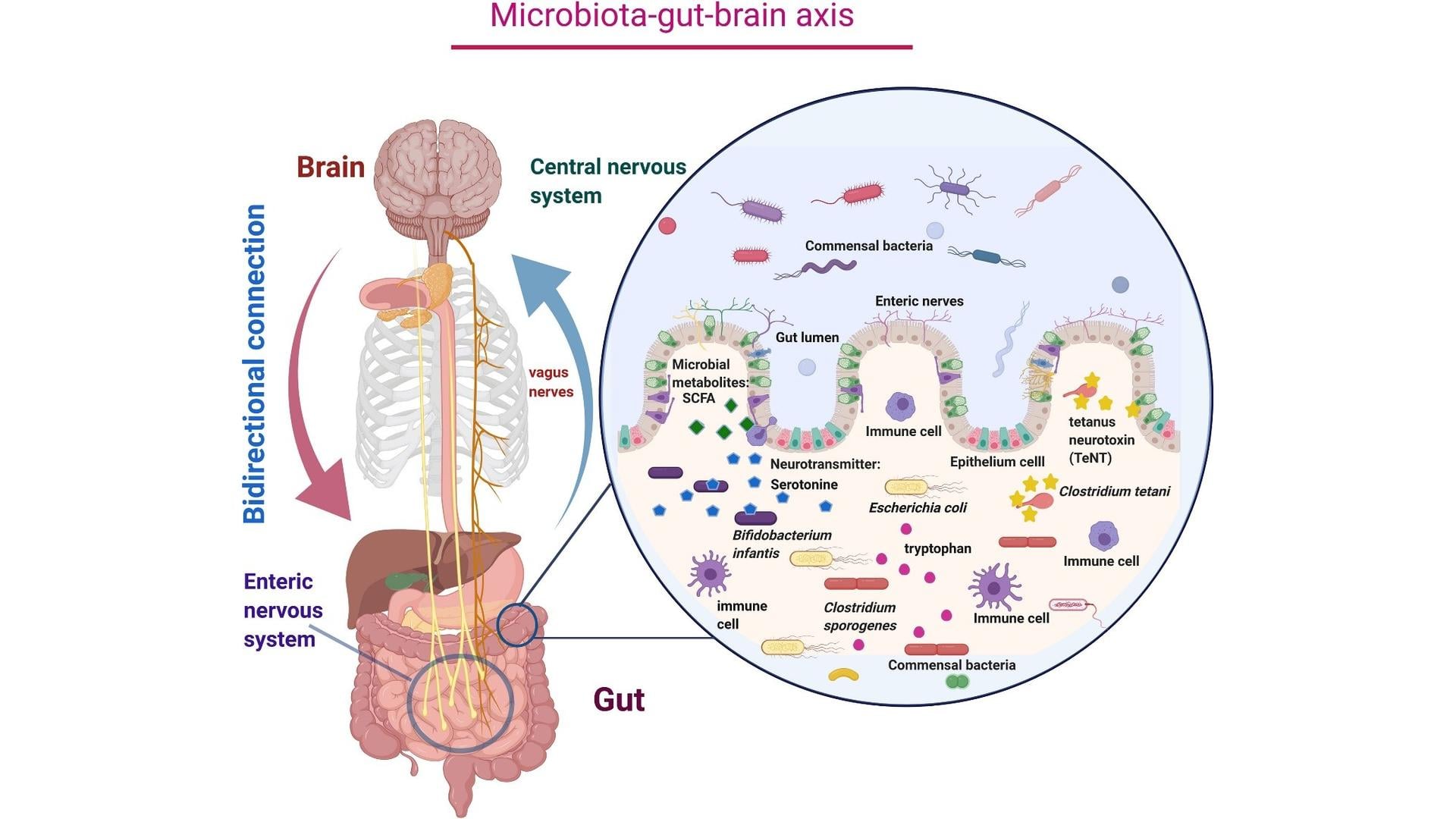
بخش اول: محور روده-مغز (Gut-Brain Axis)؛ بزرگراه اطلاعاتی بدن
محور روده-مغز یک شبکه ارتباطی دوطرفه بیوشیمیایی است. این مسیر شامل سیستم عصبی خودمختار، محور هیپوتالاموس-هیپوفیز-آدرنال (HPA) و سیستم ایمنی بدن است.
۱. عصب واگ: سیمکشی مستقیم بین شکم و مغز
عصب واگ طولانیترین عصب مغزی است که از ساقه مغز تا روده امتداد دارد. باکتریهای روده با تولید مواد شیمیایی، پیامهایی را از طریق این عصب به مغز مخابره میکنند که میتواند روی خلقوخو و رفتارهای کودک تاثیر بگذارد.
برای مطالعه بیشتر:
🔗 تغذیه و سبک زندگی در درمان اوتیسم و بیشفعالی؛ راهنمای جامع ۲۰۲۶
۲. تولید انتقالدهندههای عصبی در روده
بسیاری از مردم شگفتزده میشوند اگر بدانند بیش از ۹۰٪ سروتونین و حدود ۵۰٪ دوپامین بدن در روده تولید میشود. در کودکان مبتلا به اوتیسم، عدم تعادل میکروبی باعث اختلال در تولید این هورمونهای "شادی و تمرکز" شده و منجر به بروز رفتارهای کلیشهای و اضطراب میشود.
بخش دوم: دیسبیوز (Dysbiosis)؛ آشفتگی میکروبی در دنیای اوتیسم
تحقیقات سال ۲۰۲۵ نشان میدهند که میکروبیوم روده کودکان اوتیستیک مانند یک ارکستر از کوک خارج شده است. این پدیده را دیسبیوز مینامند.
۱. کاهش تنوع زیستی
در مغزهای با رشد معمول، تنوع باکتریایی بالا نشاندهنده سلامت است. اما در کودکان طیف اوتیسم، باکتریهای مفیدی نظیر Bifidobacterium (که مسئول کاهش التهاب است) به شدت کاهش یافتهاند.
۲. افزایش باکتریهای فرصتطلب
باکتریهایی مانند Clostridium در روده این کودکان بیش از حد تکثیر میشوند. این باکتریها متابولیتهای سمی تولید میکنند که میتواند منجر به رفتارهای تهاجمی یا بیشفعالی شود.
۳. نقش باکتری ساترلا (Sutterella)
مطالعات جدید در سال ۲۰۲۶ نشان میدهند که حضور بیش از حد باکتری ساترلا در مخاط روده کودکان اوتیستیک با مشکلات گوارشی شدید و ناتوانی در برقراری ارتباط کلامی مرتبط است.
بخش سوم: پدیده «روده نشتکننده» (Leaky Gut) و التهاب عصبی
یکی از هولناکترین کشفیات اخیر، ارتباط نفوذپذیری روده با التهاب مغزی است.
۱. وقتی سد دفاعی فرو میریزد
در حالت عادی، دیواره روده مانند یک فیلتر دقیق عمل میکند. اما در بسیاری از کودکان اوتیستیک، اتصالات بینسلولی روده شل شده و پدیده روده نشتکننده رخ میدهد.
۲. ورود سموم به خون
وقتی دیواره روده نفوذپذیر میشود، سمومی مانند لیپوپلیساکارید (LPS) وارد جریان خون میشوند. این سموم از سد خونی-مغزی عبور کرده و باعث فعال شدن میکروگلیاها (سلولهای ایمنی مغز) میشوند. نتیجه این فرآیند، التهاب عصبی مزمن است که مانع از رشد صحیح سیناپسهای مغزی میشود.
بخش چهارم: متابولیتهای میکروبی؛ پیامرسانهای پنهان رفتار
باکتریهای ما هر چه میخورند، موادی دفع میکنند که به آنها متابولیت میگویند. برخی از این مواد برای مغز حکم سم را دارند.
۱. اسیدهای چرب کوتاه زنجیره (SCFAs)
- بوتیرات: یک متابولیت قهرمان که التهاب را کاهش میدهد و در کودکان اوتیسم اغلب کم است.
- اسید پروپیونیک (PPA): تحقیقات نشان داده تزریق مقادیر بالای PPA به موشها، رفتارهای مشابه اوتیسم ایجاد میکند. این اسید در روده بسیاری از کودکان اوتیستیک بیش از حد تولید میشود.
۲. متابولیت ۴-اتیلفنیل سولفات (۴EPS)
این ماده مستقیماً توسط باکتریهای روده تولید میشود. در سال ۲۰۲۵ ثابت شد که ۴EPS با تحت تاثیر قرار دادن سلولهای اولیگودندروسیت در مغز، مانع از پیامرسانی صحیح بین نورونها شده و اضطراب اجتماعی را تشدید میکند.
بخش پنجم: جدیدترین درمانهای میکروبیوم در سالهای ۲۰۲۵ و ۲۰۲۶
امروزه از رویکردهای نوین و علمی برای بازسازی این اکوسیستم استفاده میشود.
۱. پیوند میکروبیوتای مدفوع (FMT)؛ انقلابی در درمان
پیوند مدفوع دیگر یک روش آزمایشی نیست؛ در سال ۲۰۲۶ این روش به عنوان یک درمان خط اول برای بهبود مشکلات گوارشی و رفتاری اوتیسم شناخته میشود.
- فرآیند: انتقال باکتریهای سالم از یک اهداکننده غربالگری شده به روده کودک بیمار.
- نتایج خیرهکننده: مطالعات بلندمدت نشان دادهاند که دو سال پس از FMT، علائم اصلی اوتیسم تا ۴۵٪ بهبود یافته و مشکلات گوارشی تا ۸۰٪ ریشهکن شدهاند.
۲. نسل جدید سایکوبیوتیکها (Psychobiotics)
سایکوبیوتیکها پروبیوتیکهایی هستند که اختصاصاً برای سلامت روان فرموله شدهاند.
- Lactobacillus plantarum PS128: این سویه خاص در سال ۲۰۲۵ به عنوان پرفروشترین مکمل کمکی برای اوتیسم شناخته شد، چرا که سطح دوپامین را در قشر پیشپیشانی مغز متعادل میکند.
- فرمولاسیونهای شخصیسازی شده: برخلاف پروبیوتیکهای عمومی داروخانهای، در سال ۲۰۲۶ ما بر اساس آزمایش مدفوع هر کودک، سویه مورد نیاز او را تجویز میکنیم.
۳. رژیمهای غذایی اپیژنتیک و میکروبیوم
- حذف گلوتن و کازئین (GFCF): برای کودکانی که دارای "روده نشتکننده" هستند، این رژیم میتواند بار التهابی مغز را به سرعت کاهش دهد.
- رژیم کتوژنیک تعدیل شده: این رژیم با تغییر سوخت مغز از گلوکز به کتون، محیط روده را به نفع باکتریهای مفید تغییر داده و رفتارهای تکراری را کم میکند.
برای مطالعه بیشتر:
🔗 اپیژنتیک و انقلاب در درمان اختلالات عصبی-رشدی؛ راهنمای جامع ۲۰۲۶
بخش ششم: مداخلات زیستی-رفتاری؛ ترکیب روده و آموزش
ما معتقدیم آموزشهای رفتاری (ABA) زمانی بهترین نتیجه را میدهند که بیولوژی بدن کودک آماده باشد. کودکی که از دلپیچه، یبوست مزمن یا التهاب مغزی ناشی از روده رنج میبرد، نمیتواند تمرکز کافی برای یادگیری داشته باشد.
۱. درمان "اول روده، بعد رفتار"
در پروتکلهای ۲۰۲۶ ، ابتدا وضعیت گوارشی و میکروبیوم کودک به ثبات میرسد. تجربه نشان داده است که پس از اصلاح وضعیت روده، سرعت پیشرفت کودک در جلسات کاردرمانی و گفتاردرمانی تا ۳ برابر افزایش مییابد.
بخش هفتم: سوالات متداول والدین درباره میکروبیوم و اوتیسم
آیا مصرف ماست پروبیوتیک برای درمان اوتیسم کافی است؟
خیر. مقدار باکتریهای موجود در محصولات خوراکی معمولی برای ایجاد تغییر در مغز بسیار ناچیز است. درمان نیاز به سویههای با دوز بالا و اختصاصی (Psychobiotics) دارد.
آیا تست متیلاسیون و آزمایش اسیدهای آلی ادرار (OAT) لازم است؟
بله. این آزمایشها در سال ۲۰۲۶ به ما کمک میکنند تا متوجه شویم کدام متابولیتهای باکتریایی در حال مسموم کردن سیستم عصبی کودک هستند.
پیوند مدفوع (FMT) در چه سنی موثرتر است؟
هرچه سن کمتر باشد، به دلیل انعطافپذیری بیشتر سیستم ایمنی و عصبی، نتایج درخشانتر است؛ اما تحقیقات بر روی نوجوانان نیز نتایج مثبتی نشان داده است.
بخش هشتم: نقش هوش مصنوعی (AI) در تحلیل میکروبیوم ۲۰۲۶
در سال ۲۰۲۶، از الگوریتمهای هوش مصنوعی برای تحلیل دادههای توالییابی ژنتیکی باکتریهای روده (۱۶S rRNA) استفاده میشود. این تکنولوژی به متخصصین اجازه میدهد پیشبینی کنند که هر کودک به کدام رژیم غذایی یا کدام سویه پروبیوتیک بهترین پاسخ را میدهد. این یعنی پزشکی دقیق (Precision Medicine) برای اوتیسم.
بخش نهم: سبک زندگی و عوامل محیطی موثر بر روده کودک
والدین باید بدانند که محیط خانه بر میکروبیوم کودک اثر میگذارد:
- کاهش مصرف آنتیبیوتیکهای غیرضروری: آنتیبیوتیکها مانند بمب اتمی برای باکتریهای خوب روده عمل میکنند.
- تماس با طبیعت: بازی در خاک و محیطهای طبیعی تنوع میکروبیوم کودک را بالا میبرد.
- خواب باکیفیت: بیوریتم بدن مستقیماً بر حرکت روده و سلامت باکتریها اثر میگذارد.
جمعبندی نهایی: آینده روشن است
ارتباط میکروبیوم روده و اوتیسم، بنبستهای درمانی گذشته را شکسته است. ما اکنون میدانیم که برای بهبود ذهن، باید به سلامت بدن و به خصوص دستگاه گوارش توجه کنیم. اوتیسم دیگر یک سرنوشت تغییرناپذیر نیست، بلکه وضعیتی است که با اصلاح بیولوژی بدن، میتوان شاهد شکوفایی پتانسیلهای نهفته در کودکان بود.
منابع برای مطالعه بیشتر:
محور روده-مغز
Gut microbiota analysis in children with autism spectrum disorder and their family members
سوالات متداول
پاسخ سوالات رایج درباره خدمات و درمانهای ما